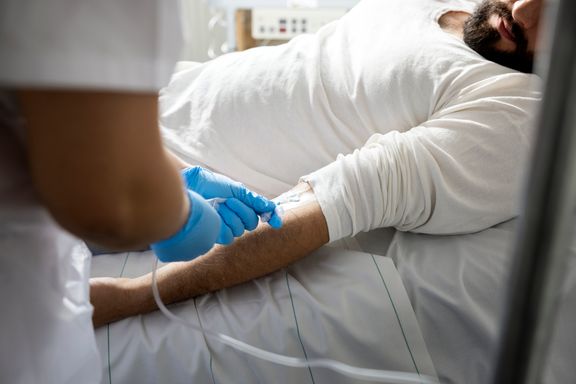
Positiva data vid pankreascancer. Novocures fas III-studie PANOVA-3 visar signifikant förlängd överlevnad vid behandling med Tumor Treating Fields (TTFields) och standardterapi.
PANOVA-3 uppnådde sitt primära mål med en statistiskt signifikant förbättring av den totala överlevnaden för patienter med icke-resektabel, lokalt avancerad pankreasadenokarcinom som behandlades i förstalinjen med TTFields i kombination med gemcitabin och nab-paklitaxel.
Novocure planerar att ansöka om regulatoriskt godkännande i USA, EU, Japan och andra viktiga marknader. Fullständiga resultat från PANOVA-3-studien kommer att presenteras vid en kommande medicinsk kongress.

Novocures fas III-studie PANOVA-3 visar signifikant förlängd överlevnad vid behandling med Tumor Treating Fields (TTFields) och standardterapi.
Novocure announces that the pivotal, Phase 3 PANOVA-3 trial met its primary endpoint, demonstrating a statistically significant improvement in median overall survival (mOS) versus control. PANOVA-3 evaluated the use of Tumor Treating Fields (TTFields) therapy concomitantly with gemcitabine and nab-paclitaxel as a first-line treatment for unresectable, locally advanced pancreatic adenocarcinoma.
“As a researcher and clinician, I have experienced the challenges of developing treatments in pancreatic cancer. It is exciting to see the PANOVA-3 trial achieve the positive primary endpoint of overall survival, a landmark outcome for this field,” said Vincent Picozzi, M.D., medical oncologist and investigator in the PANOVA-3 trial. “These data for Tumor Treating Fields are very promising, especially in this difficult to treat patient population.”
In the intent-to-treat population, patients treated with TTFields therapy concomitant with gemcitabine and nab-paclitaxel had an mOS of 16.20 months compared to 14.16 months in patients treated with gemcitabine and nab-paclitaxel alone, a statistically significant 2.0-month improvement (hazard ratio=0.819; P=0.039) (N=571). The survival rate benefit for patients treated with TTFields therapy increased over time with a 13% improvement in the overall survival rate at 12 months and a 33% improvement in survival rate at 24 months. TTFields therapy was well-tolerated, and safety was consistent with prior clinical studies.
“PANOVA-3 is the first and only Phase 3 trial to demonstrate a statistically significant benefit in overall survival specifically in unresectable, locally advanced pancreatic cancer, and is Novocure’s third positive Phase 3 clinical trial in the last two years,” said Nicolas Leupin, M.D., PhD, Chief Medical Officer, Novocure. “We are grateful to the patients and investigators for their participation in the trial, and we look forward to sharing the full data at an upcoming medical conference.”
Novocure plans to file for regulatory approval of TTFields in unresectable, locally advanced pancreatic adenocarcinoma based on PANOVA-3 and plans to submit the PANOVA-3 results for presentation at an upcoming medical congress.
Novocure continues to follow patients in its Phase 2 PANOVA-4 trial, exploring the use of TTFields therapy together with atezolizumab, gemcitabine and nab-paclitaxel for the treatment of metastatic pancreatic cancer. PANOVA-4 has completed enrollment with data anticipated in 2026.
About PANOVA-3
PANOVA-3 is a prospective, randomized, open-label, controlled Phase 3 clinical trial designed to test the efficacy and safety of Tumor Treating Fields (TTFields) therapy used concomitantly with gemcitabine and nab-paclitaxel, as a first-line treatment of locally advanced pancreatic adenocarcinoma. Patients were randomized to receive either TTFields therapy concomitant with gemcitabine and nab-paclitaxel or gemcitabine and nab-paclitaxel alone.
The primary endpoint is overall survival. Secondary endpoints include progression-free survival, local progression-free survival, objective response rate, one-year survival rate, quality of life, pain-free survival, puncture-free survival, resectability rate, and toxicity.
A total of 571 patients were enrolled in the study, randomized 1:1 and followed for a minimum of 18 months.
About PANOVA-4
PANOVA-4 is an international, multi-center Phase 2 clinical trial designed to test the safety and efficacy of Tumor Treating Fields (TTFields) therapy together with atezolizumab, gemcitabine and nab-paclitaxel for the treating of metastatic pancreatic cancer. The primary endpoint is disease control rate. Secondary endpoints include overall survival, progression-free survival, one-year survival rate, objective response rate, progression-free survival at six months, duration of response and toxicity. The study is designed to enroll 76 patients.
About Pancreatic Cancer
Pancreatic cancer is one of the most lethal cancers and is the third most frequent cause of death from cancer in the U.S.[1] While overall cancer incidence and death rates are remaining stable or declining, the incidence and death rates for pancreatic cancer are increasing.[2] It is estimated that approximately 67,000 patients are diagnosed with pancreatic cancer each year in the U.S.[3] Pancreatic cancer has a five-year relative survival rate of just 13%.[4]
Physicians use different combinations of surgery, radiation and pharmacological therapies to treat pancreatic cancer, depending on the stage of the disease. For patients with locally advanced pancreatic cancer involving encasement of arteries but no extra-pancreatic disease, the standard of care is surgery followed by chemotherapy with or without radiation. Unfortunately, most locally advanced cases are diagnosed once the cancer is no longer operable, generally leaving chemotherapy with or without radiation as the only treatment option.
About Tumor Treating Fields
Tumor Treating Fields (TTFields) are electric fields that exert physical forces to kill cancer cells via a variety of mechanisms. TTFields do not significantly affect healthy cells because they have different properties (including division rate, morphology, and electrical properties) than cancer cells. These multiple, distinct mechanisms work together to target and kill cancer cells. Due to these multimechanistic actions, TTFields therapy can be added to cancer treatment modalities in approved indications and demonstrates enhanced effects across solid tumor types when used with chemotherapy, radiotherapy, immune checkpoint inhibition, or targeted therapies in preclinical models. TTFields therapy provides clinical versatility that has the potential to help address treatment challenges across a range of solid tumors.
To learn more about TTFields therapy and its multifaceted effect on cancer cells, visit tumortreatingfields.com.